УДК 617-089+616-089.843+616.314.17-008-002-06
Сравнительный анализ структуры поверхности и ее химического состава у разных систем дентальных имплантатов и их влияние на уровень сенсибилизации организма
Камалов Р.Х.1, Лихота А.Н.1, Коваленко В.В.1, Тинков В.А.2, Горобец Е.В.1, Кинчур Н.И.1, Розова Е.В.3
Украинская военно-медицинская академия1, Институт металлофизики НАН Украины им. Курдюмова2, Институт физиологии им. А.А.Богомольца НАН Украины3, Киев
На сегодняшний день дентальная имплантация является ведущим методом восстановления жевательной эффективности у пациентов с вторичной адентией. Зубные имплантаты чаще всего изготавливаются из биоинертных материалов (титан, цирконий, корундовая керамика), которые способствуют полноценной остеоинтеграции (сращению поверхности зубного имплантата с костной тканью), а также устойчивых к коррозии, не вызывающих аллергических реакций, хорошо совместимых с материалами, из которых изготавливаются супраструктуры. Для достижения остеоинтеграции определяющими факторами являются: биосовместимость имплантата; форма и качество поверхности имплантата. Поверхность используемого имплантата должна обладать высокой чистотой и достаточной шероховатостью для обеспечения адекватной остеоинтеграции, за счет улучшения контакта кости и имплантата, что достигается благодаря увеличенной топографии его поверхности [2,6,11,12,17].
Эффективность процесса репаративной регенерации является ключевым моментом для обеспечения механической целостности соединения имплантата и кости. При этом показано, что грубые поверхности имплантатов с различной топографией демонстрируют лучшее сцепление с костью. Бусер и др. обнаружили, что увеличение грубости поверхности имплантата напрямую связано с увеличением поверхности сцепления с костью. Было выдвинуто предположение о том, что грубая поверхность имплантата является одним из самых важных факторов, влияющих на успех имплантации. Однако, структура поверхности имплантата является не единственным критерием, необходимым для оптимальной остеоинтеграции. Комбинация рисунка на поверхности имплантата, что характеризует ее топографию, в комплексе с уровнем химической чистоты поверхности обеспечивают оптимальную ответную реакцию имплантационного ложа кости [2,3,13,14].
Тем не менее, при использовании современных систем имплантатов, как отечественных, так и зарубежных фирм производителей в 3-7% случаев возникают различные осложнения в постимплантационном периоде, которые не связаны с наличием общесоматической патологии у пациентов, с нарушением хирургического протокола или с осложнениями ортопедического этапа лечения [2,4,9,16]. Следовательно, выявленные осложнения могут быть связаны именно с качеством поверхности внутрикостной части дентальных имплантатов различных систем.
В связи этим, целью данного исследования являлось изучение топографии и химического состава внутрикостной части поверхности дентальных имплантатов разных фирм производителей.
Материалы и методы
В работе проведено сравнительное изучение качества поверхности 5 различных систем дентальных имплантатов: α-dent, α-bio и NOVA(Израиль), Densply (Ankylos) (Германия), NIKО-Lux (Россия). Качество внутрикостных поверхностей всех перечисленных систем имплантатов и спектр их химического состава изучали с помощью растрового электронного микроскопа Jeol (Япония) до их введения в зону имплантации. Имплантаты систем α-dent и NOVA были исследованы также после их отторжения из костной ткани.
Определение уровня микробной сенсибилизации к стафилококку проводили путем постановки теста показателя повреждения нейтрофилов крови – ППН по В.А. Фрадкину [8]. Полученные показатели обработаны методом вариационной статистики с вычислением критериев Стьюдента. Показатели считали достоверными при р < 0,05.
Результаты и обсуждение
Проведенные исследования позволили охарактеризовать химический состав и структуру указанных имплантатов.
Как известно, все металлы, используемые в медицине, делятся на 3 основные группы: 1) токсические металлы (ванадий, никель, хром, кобальт); 2) промежуточные металлы (железо, золото, алюминий); 3) инертные металлы (титан, цирконий). В настоящее время дентальные имплантанты изготавливаются из титана и его сплавов, поскольку титан является биосовместимым и некоррозийным материалом. Поэтому, внутрикостная поверхность дентальные имплантанты не должна содержать посторонних примесей, либо включать минимальное количество контаминатов, появление которых может быть результатом физической и/или химической обработки поверхности с целью увеличение грубости поверхности имплантата [5,7,10,19].
При изучении имплантатов системы α-dent было выявлено, что их внутрикостная поверхность содержит значительное количество контаминатов (Табл. 1).
Таблица 1 – Пример химического состава поверхности имплантата α-dent
| Элемент | Весовой % | Атомный % |
| O K | 50.47 | 69.96 |
| Na K | 0.67 | 0.65 |
| Mg K | 4.66 | 4.25 |
| Al K | 6.48 | 5.33 |
| Si K | 6.98 | 5.51 |
| K K | 1.88 | 1.07 |
| Ca K | 0.37 | 0.20 |
| Ti K | 25.26 | 11.69 |
| V K | 1.43 | 0.62 |
| Fe K | 1.80 | 0.71 |
| Итого | 100.00 | 100.00 |
В дальнейшем внимание будет уделяться анализу наличия на поверхности имплантата титана (Ti), как материала, из которого изготовлен имплантат, а также алюминия (Al) и железа (Fe), относящихся к группе промежуточных, и ванадия (V), относящегося к группе токсичных для организма.
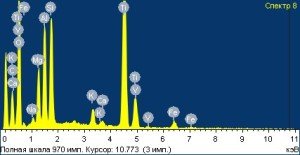
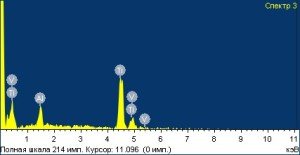
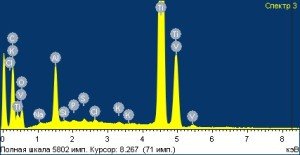
В зависимости от исследуемого участка поверхности концентрации металлов значительно варьировали: Ti – от 2,00 до 94,40 весовых %; Al – от 1,55 до 49,58 весовых %; Fe – от 0,44 до 1,80 весовых % и V – от 1,00 до 5,13 весовых % (Рис. 1).
Рисунок 1 – Структура поверхности и спектр ее химического состава у имплантата системы α-dent.
Как видно из приведенного рисунка, поверхность имплантата имеет неоднородную топографию внутрикостной части, что может препятствовать равномерной абсорбции белков, оптимальному прикреплению к поверхности материала волокон фибрина, коллагена, адгезии остеогенных клеток (фибро- и остеобластов), а также приводить к выраженной мозаичности синтеза специфических белков, в том числе факторов роста, что снижает площадь костной интеграции.
Наличие на поверхности исследуемых имплантатов значительного количества алюминия обусловливается, некачественной воздушно-абразианой обработкой внутрикостной поверхности титановой основы имплантата с помощью порошка алюмооксидной керамики без последующей эффективной очистки с помощью химического травления поверхности. Присутствие на поверхности имплантата Al в концентрациях, превышающих 0,1%, токсически влияет на обмен веществ, в частности минеральный, конкурируя с ионами кальция и магния, оказывает непосредственное воздействие на рост и размножение клеток посредством негативного действия на клеточную мембрану, т.е. препятствует еффектвному течению процессов репаративной регенерации в зоне имплантации [5,7]. Дополнительный вклад в нарушение процессов остеоинтеграции вносит наличие железа, примесь которого не должна присутствовать на поверхности имплантатов.
Особое внимание следует обратить на выявленные в ходе исследования контоминаты ванадия, являющегося для организма токсичным металлом. Хотя физиологическая роль ванадия недостаточно изучена, полагают, что ванадий участвует в регуляции метаболизма, в частности, тканей костей и зубов, но при избыточном поступлении его в организм тормозит фосфорилирование и синтез АТФ, влияя на активность моноаминоксидазы, является геморрагически-эндотелиотоксичным ядом. Такие особенности его воздействия приводят к нарушению трофических процессов в тканях организма, в частности в тканях пародонта, и нарушают тем самым течение процессов репаративной регенерации в зоне имплантации [1,10,15].
При изучении имплантатов системы NOVA так же, как и в предыдущем случае, было выявлено, что их внутрикостная поверхность содержит значительное количество контаминатов (Табл. 2).
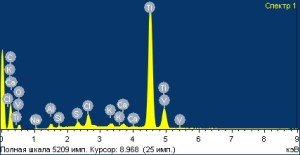
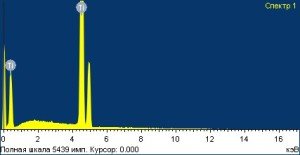
На внутрикостной поверхности исследуемых имплантатов выявлено наличие: Ti – от 1,70 до 82,75 весовых %; Al – от 0,80 до 62,82 весовых %; Fe – от 0,14 до 0,20 весовых % и V – от 0,31 до 1,05 весовых % (Рис. 2). Контаминаты алюминия располагались мозаично по поверхности имплантата, железо присутствовало лишь в виде следов, а количество ванадия на поверхности имплантатов было в среднем в 4,5 раза меньше, чем выявлялось при исследовании имплантатов α-dent.
Таблица 2 – Пример химического состава поверхности имплантата NOVA
| Элемент | Весовой % | Атомный % |
| O K | 11.99 | 19.45 |
| Na K | 1.27 | 1.43 |
| Al K | 2.18 | 2.09 |
| Si K | 0.32 | 0.30 |
| S K | 0.26 | 0.21 |
| Cl K | 1.25 | 0.91 |
| K K | 0.36 | 0.24 |
| Ca K | 1.44 | 0.93 |
| Ti K | 59.26 | 32.11 |
| V K | 2.74 | 1.40 |
| Итого | 100.00 | 100.00 |
А Б
Рисунок 2 — Структура поверхности и спектры ее химического состава у имплантата системы NOVA
Как видно из приведенного рисунка, поверхность имплантата имеет более однородную топографию внутрикостной части, чем имплантаты предыдущей системы, однако недостаточно развитую поверхность для обеспечения эффективной остеоинтеграции. Несмотря на то, что количество Fe и V на внутрикостной поверхности имплантатов было значительно меньше, что выгодно отличает имплантаты системы NOVA от системы α-dent, контаминаты алюминия на некоторых исследуемых участках занимали подавляющую удельную площадь поверхности, что в последующем не позволяет достичь оптимальной площади костной интеграции (Рис. 2 А,Б).
При изучении имплантатов системы α-bio, было выявлено, что их внутрикостная поверхность содержит незначительное количество контаминатов (Табл. 2).
Таблица 3 – Пример химического состава поверхности имплантата α-bio
| Элемент | Весовой % | Атомный % |
| Al K | 5.40 | 9.23 |
| Ti K | 94.10 | 90.63 |
| V K | 0.50 | 0.45 |
| Итого | 100.00 | 100.00 |
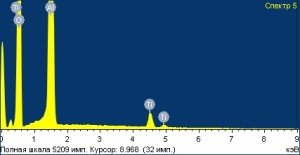
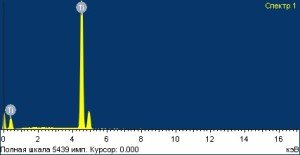
На внутрикостной поверхности исследуемых имплантатов выявлено наличие: Ti – от 36,10 до 88,51 весовых %; Al – от 0,80 до 5,40 весовых % и V – от 0,10 до 0,51 весовых %, т.е., следовые количества (Рис. 3).
Рисунок 3 — Структура поверхности и спектры ее химического состава у имплантата системы α-bio.
Видно, что поверхность имплантата имеет достаточно однородную и грубую топографию внутрикостной части, что в комплексе с незначительным количеством контаминатов на ее поверхности способно обеспечить достаточно эффективную остеоинтеграцию в зоне имплантации.
Несмотря на то, что имплантаты системы α-bio в ходе технологического формирования поверхности подвергались кислотной протравке, призванной удалять посторонние примеси с внутрикостной титановой поверхности, на ней выявлялось определенное количество контаминатов алюминия. Поскольку алюминий и его соединения обладают политропным действием на организм, выраженность которого не находится в прямой зависимости от его концентрации, при проведении имплантации следует принимать во внимание возможность возникновения осложнений в постимплантационном периоде, вызванных сенсибилизацией им организма [5,7].
При изучении имплантатов системы Densply (Ankylos) было выявлено, что их внутрикостная поверхность не содержит контаминатов, внутрикостная поверхность состоит исключительно из титана. Кроме того, следует отметить, что поверхность имплантата, за счет химического травления, имеет высоко структурированную топографию, что значительно увеличивает удельную площадь поверхности, взаимодействующей с костью, в результате чего повышается эффективность остеоинтеграции (Рис. 4).
Рисунок 4 — Структура поверхности и спектры ее химического состава у имплантата системы Densply (Ankylos).
При изучении имплантатов системы NIKО-Lux показано, что их внутрикостная поверхность на 100% представлена титаном. Имплантаты данной системы представляют собой пример позитивного влияния кислотного травления на поверхность, не содержащую контаминатов (Рис. 5). Такая обработка приводит к возрастанию глубины микровпадин поверхности имплантатов, образованию равномерного микрогеометрического рельефа, что значительно увеличивает удельную площадь, контактирующей с костью, и сопровождается оптимизацией остеоинтеграции в зоне имплантации и снижением уровня механического напряжения в окружающей имплантат кости.
Рисунок 5 — Структура поверхности и спектры ее химического состава у имплантата системы NIKО-Lux.
Известно, что остеоинтеграция — это не изолированное явление и во многом зависит от свойств материалов, из которых изготовлен имплантат. При этом в пространстве между поверхностью имплантата и костной тканью не образуется фиброзная или хрящевая ткань [18]. Остеоинтегрированые имплантаты характеризуются с помощью микроскопического анализа как субстанция, располагающаяся в непосредственном контакте с костной тканью, без каких либо признаков на присутствие соединительной ткани между костью и имплантатом [6,13].
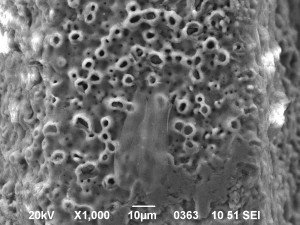
При изучении отторгнутых имплантатов систем α-dent и NOVA установлено, что их внутрикостная поверхности была покрыта органическими остатками (Рис. 5), в составе которых присутствовали такие элементы как фосфор и сера и полностью отсутствовал кальций (Табл. 4), что характерно для фиброзной и хрящеподобной тканей, а не для минерализованной кости. Подобная ткань может образовываться как ответ на наличие на поверхности имплантатов контаминатов, содержащих токсичные металлы.
Рисунок 5 — Структура поверхности и спектры ее химического состава у отторгнутого имплантата.
Таблица 4 – Пример химического состава поверхности отторгнутого имплантата
| Элемент | Весовой % | Атомный % |
| O K | 19.74 | 41.23 |
| Na K | 0.31 | 0.45 |
| Al K | 4.51 | 5.59 |
| Si K | 0.07 | 0.08 |
| P K | 0.15 | 0.16 |
| S K | 0.24 | 0.25 |
| Cl K | 0.21 | 0.19 |
| K K | 0.20 | 0.17 |
| Ti K | 70.91 | 49.47 |
| V K | 3.66 | 2.40 |
| Итого | 100.00 | 100.00 |
Рассмотрение вопросов имплантации, касающихся клинической части проблемы (выбор показаний к операции, выбор конструкции имплантата и ортопедической конструкции), доминирует над решением вопросов индивидуальной биосовместимости как основополагающих предпосылок к успешному результату лечения в целом [14]. Определенная доля неудач может наблюдаться из-за недооценки таких сложно контролируемых факторов, как реакция на материал, сенсибилизация пациента [4, 10, 19]. Правильность такого заключения была подтверждена в ходе проведенного исследования. Было выявлено, что при применении для дентальной имплантации систем α-dent и NOVA, содержащих значительное количество контаминатов алюминия, железа и ванадия, около 5% установленных имплантатов отторгаются в течение первых 3-х месяцев. Одной из причин отторжения может быть сенсибилизация организма пациентов, обусловленная введением в организм токсичных и промежуточных металлов.
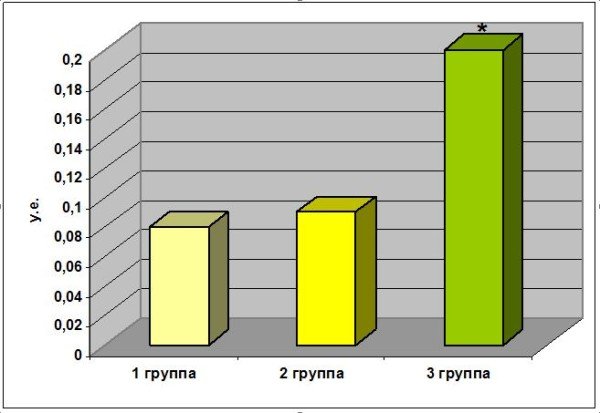
Показано, что в период остеоинтеграции (в течение 3-х месяцев после имплантации) у всех обследуемых пациентов, которым были установлены имплантанты систем α-bio, Densply (Ankylos) и NIKО-Luxпоказатели повреждения нейтрофилов достоверно не отличались от характерных для здоровых лиц (Рис.6).
Рисунок 6 — Уровень микробной сенсибилизации к стафилококку. 1 группа – контрольная, 2 группа – первые 3 месяца после имплантации, 3 группа — первые 3 месяца после имплантации при наличии отторжения имплантата. * — р<0,05 относительно контрольной группы.
У 5,2% больных с частичными дефектами зубного ряда, которым проводили имплантацию с помощью систем α-dent и NOVA, эти показатели определялись на значительно (в 2,5 раза) повышенном уровне. Именно у данной категории больных наблюдался периимплантит, в результате которого произошло отторжение имплантатов.
Выводы
Проведенные исследования показали, что на внутрикостной поверхности имплантатов систем α-dent и NOVA содержится значительное количество контаминатов, содержащих токсичные и промежуточные металлы – алюминий, железо, ванадий — не обладающих биоинертными свойствами.
Наличие значительного количества контаминатов на внутрикостной поверхности имплантатов систем α-dent и NOVA является одной из причин развития периимплантита, обусловленного сенсибилизацией организма, приводящего к отторжению имплантатов в 5,2% случаев, что требует предварительного выявления уровня сенсибилизации организма пациента в предимплантационном периоде.
Видно, что поверхность имплантата имеет достаточно однородную и грубую топографию внутрикостной части, что в комплексе с незначительным количеством контаминатов на ее поверхности способно обеспечить достаточно эффективную остеоинтеграцию в зоне имплантации.
Несмотря на то, что имплантаты системы α-bio содержат незначительное количество контаминатов алюминия и ванадия, обладающих политропным действием на организм, при проведении имплантации следует принимать во внимание возможность возникновения осложнений в постимплантационном периоде.
Внутрикостные поверхности имплантатов систем Densply (Ankylos) и NIKО-Lux состоит исключительно из титана. Кроме того, поверхность имплантатов системы NIKО-Luxхарактеризуется равномерным разработанным микрогеометрическим рельефом, что значительно увеличивает удельную площадь, контактирующую с костью, и способствует оптимизации процессов остеоинтеграции.
Полученные результаты показали, что при использовании для дентальной имплантации имплантатов систем Densply (Ankylos) и NIKО-Lux не наблюдается отторжения имплантатов, что свидетельствует об адекватной остеоинтеграции в зоне имплантации и отсутствии сенсибилизации организма пациентов.
Литература
- Горкин В.З. Аминоксидазы и их значение в медицине. М.:Медицина, 1981. — 336 с.
- Григорьян А.С., Топоркова А.К. Опыт исследования процессов интеграции имплантационных материалов в костной ткани // Всероссийское совещание «Биокерамика в медицине».- М.: Б.и., 2006. -С.88-89.
- Кулаков А.А., Григорьян А.С., Филонов М.Р., Штанский Д.В., Топоркова А.К. Влияние различных по химическому составу покрытий интраоссальных титановых имплантатов на их интеграцию в кость // Росс. вестн. дент. имплантол. — 2007. – Т. 15/16, № 3/4. — С.10-15.
- Майбородин И.В., Якушенко В.К., Майбородина В.И. Взаимодействие никелид-титанового имплантата с тканями человека // Архив патологии. — 2002. — № 2. — С. 50–52.
- Моисеев С.В. Алюминийсодержащие препараты: риск превышает пользу // Гастроэнтерология. — 2006. — № 2. — С.27-30.
- Сунг Ам Чо, Санг-Кио Юнг. Усилие при выкручивании титановых имплантатов с поверхностью, обработанной лазером, из большеберцовой кости кролика // Biomaterials. – 2003. — №24. – Р. 4859-4863.
- Харламов О.В. Экология и токсикология алюминия //Гигиена и санитария.- 2004. — №3. — С. 73-75.
- Фрадкин В.А. Диагностика аллергии реакциями нейтрофилов крови. – М.: Медицина. – 1985. – 175 с.
- Штанский Д.В., Петржик М.И., Башкова И.А. и др. Адгезионные, фрикционные и деформационные характеристики покрытий Ti-(Ca,Zr)-(C,N,O,P) для ортопедических и зубных имплантов // Физика твердого тела.- 2006. — Т.48, №7. — С. 1231-1238.
- Budinger L., Hertl M. Immunological mechanisms in hypersensitivity reactions to metal ions: an overview // Allergy. — 2000. — Vol. 55, № 1. — P. 108–115.
- Cordioli G., Majzoub Z., Piatelli A., Scarano A. Removal torque and histomorphometric investigation of 4 different titanium surfaces // Int. J. Oral. Maxillofac. Implants. – 2000. – Vol.15, N 5. – P. 668–674.
- Gaggl A., Schultes G., Muller W.D., Karcher H. Scanning electron microscopical analysis of laser-treated titanium implants surfaces — a comparative study // Biomaterials. – 2000. – Vol.21, N 9. – P.1067–1073.
- Itala A.I., Ylanen H.O., Ekholm C., Karlsson K.H., Aro H.T.. Pore diameter of more than 100 mm is not requisite for bone ingrowths in rabbits // J. Biomed. Mater. Res. – 2000. — Vol.58, N 5. – P.679–683.
- Kupp L.I. Поверхности имплантатов и костеобразование. Клинический отчет // Стоматолог. — 2002. — № 3. — С. 22–23.
- LemonsJ., Anabtawi M., Beck P. et al. Histomorphometry of Explanted Dental Implants // IADR.- New Orleans, 2007.- № 3.
- Mustafa K., Wennerberg A., Wroblewski J., Hultenby K., Lope B.S., Arvidson K. Determining optimal surface roughness of TiO (2) blasted titanium implant material for attachment, proliferation and differentiation of cells derived from human mandibular alveolar bone // Clin. Oral. Implant. Res. – 2001. – Vol.12, N 4. – P.515–525.
- Shigematsu I., Nakamura M., Saitou N., Shimojima K. Surface hardening treatment of pure titanium by carbon dioxide laser // J. Mater. Sci. Lett. – 2000. – Vol.19, N 9. – P.967–970.
- Sul Y.T. On the bone response to oxidized titanium implants. Ph.D. thesis, Department of Biomaterials / Handicap Research, University of Gothenburg, Sweden; 2002.
- Thomas P., Summer B., Sander C.A., Przybilla B., Thomas M., Naumann T. Intolerance if osteosyntesis material: evidence of dichromate contact allergy with concomitant oligoclonal T-cell infiltrate and TH1-type cytokine expression in the peri-implantar tissue // Allergy. — 2000. — Vol. 55., N8. — P. 969–972.
Сравнительный анализ структуры поверхности и ее химического состава у разных систем дентальных имплантатов и их влияние на уровень сенсибилизации организма
Камалов Р.Х., Лихота А.Н., Коваленко В.В., Тинков В.А., Горобец Е.В., Кинчур Н.И., Розова Е.В.
Резюме
В работе проведено сравнительное изучение качества поверхности 5 различных систем дентальных имплантатов: α-dent, α-bio и NOVA(Израиль), Densply (Ankylos) (Германия), NIKО-Lux (Россия). Показано, что наличие значительного количества контаминатов на внутрикостной поверхности имплантатов систем α-dent и NOVA является одной из причин развития периимплантита, обусловленного сенсибилизацией организма, приводящего к отторжению имплантатов в 5,2% случаев. Внутрикостные поверхности имплантатов систем Densply (Ankylos) и NIKA-Lux состоит исключительно из титана. Кроме того, поверхность имплантатов системы NIKA-Lux характеризуется равномерным разработанным микрогеометрическим рельефом, что значительно увеличивает удельную площадь, контактирующую с костью, и способствует оптимизации процессов остеоинтеграции.
Ключевые слова: дентальные имплантаты, внутрикостная поверхность имплантатов, контаминаты, периимплантит, сенсибилизация.
Comparative analysis of surface structure and her chemical composition at the different systems of dental implants and their influence on the level of sensibilization of organism
Kamalov R.Ch., Lichota A.N., Kovalenko V.V., Tinkov V.A., Gorobets E.V., Kinchur N.I., Rozova E.V.
Summary
The comparative study of quality of surface is in-process conducted 5 different systems of dental implants: α-dent, α-bio and NOVA (Israel), Densply (Ankylos) (Germany), NIKО — Lux (Russia). It was shown that presence of far of contaminats on the intraosseous surface of implants of the systems α-dent and NOVA is one of the reasons of development of periimplantitis, conditioned to the organism sensibilization and resulting in tearing away of implants in 5,2% cases. Intraosseous surfaces of implants of the systems of Densply (Ankylos) and NIKA — Lux consists exceptionally of titan. In addition, surface of implants of the system NIKA — Lux is characterized by the even worked out microgeometrical relief, which considerably increases a specific area contacting by a bone-in, and assists to the optimization of processes of osteointegration.
Key words: dental implants,intraosseous surfaces of implants, contaminats, periimplantitis, sensibilization.